Titrering af stærk monohydron syre med stærk base
Titrering af stærk monohydron syre
HCl er et eksempel på en stærk monohydron syre. Vi siger, vi ikke kender koncentrationen af en HCl-opløsning, og at vi gerne vil bestemme koncentrationen ved at titrere med en 0,1 M NaOH-opløsning.
Titreringsreaktionen
Titreringsreaktionen for denne titrering kan opskrives på flere måder.
Version 1 af titreringsreaktionen:
Man kan for eksempel opskrive den på følgende måde:
HCl(aq) + OH-(aq) → Cl-(aq) + H2O(l)
Vi bemærker, at syren (HCl) og basen (OH-) reagerer i forholdet 1:1.
Version 2 af titreringsreaktionen:
Man kan også opskrive titreringsreaktionen således:
HCl(aq) + NaOH(aq) → NaCl(aq) + H2O(l)
Vi bemærker, at i denne version er tilskuerionen, Na+, skrevet med i titreringsreaktionen.
Version 3 af titreringsreaktionen:
Alternativt kan man også opskrive titreringsreaktionen således:
H3O+(aq) + OH-(aq) → H2O(l) + H2O(l)
Her har vi erstattet HCl med H3O+. Det kan vi tillade os, fordi HCl – allerede før titreringen er startet – har afgivet en hydron til H2O, hvorved der dannes H3O+. Og dermed er det faktisk H3O+, der reagerer med OH-, når titreringen starter. Alle tre versioner af titreringsreaktionen er gode at have forståelse for, selvom de dybest set bare beskriver det samme.
Titrerkurven
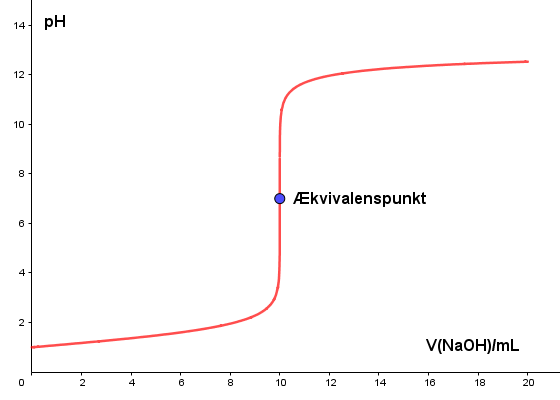
Titrerkurven for denne titrering vil typisk se cirka således ud:
Ud ad x-aksen har vi volumen af tilsat NaOH målt i mL, og op ad y-aksen har vi pH-værdien. pH starter altså med at være relativt lav, hvorefter pH begynder at stige, i takt med at der dryppes mere og mere NaOH ned i opløsningen. Omkring ækvivalenspunktet stiger pH kraftigt. Ækvivalenspunktet er det punkt, hvor det sidste syremolekyle reagerer.
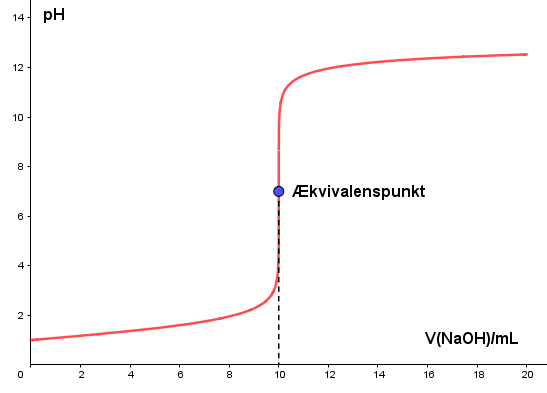
Ækvivalenspunktet
Ækvivalenspunktet er normalt det vigtigste punkt ved en titrering:
Når vi når ækvivalenspunktet, skal vi normalt stoppe titreringen og aflæse på buretten, hvor meget NaOH vi har tilsat. I dette tilfælde er der blevet tilsat cirka 10 mL. Vi kan bruge denne aflæsning til at bestemme koncentrationen af syren i den oprindelige o...