Her får du vores komplette guide til reaktionshastighed. Reaktionshastighed handler om, hvor hurtigt en reaktion forløber. Guiden dækker alt det du skal vide, uanset om du har Kemi B eller Kemi A.
Vær opmærksom på, at reaktionshastighed også går under navnet reaktionskinetik.
Her får du et uddrag af siden om sammenligning af reaktionshastigheden for et produkt og en reaktant
Lad os nu se et eksempel med en rigtig kemisk reaktion. Dibrom, Br2, kan dannes ud fra bromidionen, Br-, og bromationen, BrO3- ved denne redoxreaktion:
5Br-(aq) + BrO3-(aq) + 6H+(aq) → 3Br2(aq) + 3H2O(l)
Herunder ser du graferne for henholdsvis reaktanten, [BrO3-] (den røde graf) og produktet, [Br2] (den blå graf) som funktion af tiden:
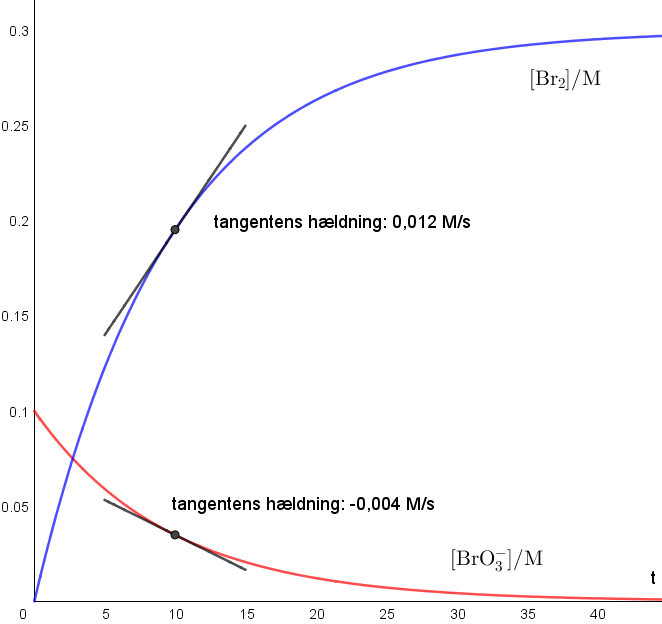
Denne graf ville være et typisk bilag til den mundtlige eksamen i Kemi B og Kemi A. Hvad skal du sige til sådan et bilag?
Vi bemærker, at vi på koefficienterne i reaktionsskemaet kan se, at BrO3- og Br2 reagerer i forholdet 1:3. Dette reaktionsforhold kan også ses på de to grafer.
Den røde graf repræsenterer reaktanten, [BrO3-], som funktion af tiden. Vi kan se, at denne graf er aftagende, hvilket passer godt med at der er tale om en reaktant. Det ser ud som om startkoncentrationen var 0,1 M, altså [BrO3-]=0,1 M.
Den blå graf repræsenterer produktet, [Br2], som funktion af tiden. Vi kan se, at denne graf er voksende, hvilket passer godt med at der er tale om et produkt. Slutkoncentrationen for produktet ser ud til at være cirka 0,3 M, altså [Br2]=0,3 M, hvilket er 3 gange så meget som startkoncentrationen af BrO3- . Dette passer godt med, at reaktionsforholdet er 1:3. For hver gang, der omdannes 1 BrO3- , dannes der 3 Br2.
Til tidspunktet t=10 sekunder er tangenthældningen for reaktanten -0,004 M/s. Da man ikke kan have en negativ reaktionshastighed, tager vi den numeriske værdi, og får dermed en reaktionshastighed for BrO3- på 0,004 M/s.
Til tidspunktet t=10 sekunder er tangenthældningen for produktet 0,012 M/s. Reaktionshastigheden for Br2 til dette tidspunkt er altså 0,012 M/s, som er tre gange så meget som reaktionshastigheden for BrO3-. Dette skyldes reaktionsforholdet på 1:3 ...


